Modificación genetica
Un organismo modificado genéticamente (abreviado OMG, OGM o GMO, este último del inglés Genetically Modified Organism) es aquel cuyo material genético es manipulado en laboratorios donde ha sido diseñado o alterado deliberadamente con el fin de otorgarle alguna característica específica. Comúnmente se los denomina transgénicos y son creados artificialmente en laboratorios por ingenieros genéticos.
Usos
La primera medicina genético dirigida era ser humano sintético insulina, aprobado por Estados Unidos Administración del alimento y de la droga en 1982. Los científicos utilizaron las bacterias en las cuales insertaron los plasmids que contenían las direcciones para la insulina, ellos podían entonces utilizar las bacterias para producir y para cosechar la insulina artificial. Otro uso temprano de la ingeniería genética era crear la hormona humana del crecimiento como reemplazo para una droga que fue extraída previamente de ser humano cadavers. En 1987 el FDA aprobó el primer genético dirigido vacuna para los seres humanos, para hepatitis B. Puesto que éstos temprano las aplicaciones de la tecnología en medicina, el uso del GM se han ampliado gradualmente para proveer un número de otras drogas y vacunas. Uno de los usos más conocidos de la ingeniería genética es la creación de organismos genético modificados (GMOs) por ejemplo los alimentos y los vehículos que resisten el parásito y las bacterias infección y tienen frescura más larga que de otra manera.
Hay potencialmente trascendental biotechnological usos del GM, por ejemplo oral vacunas producido naturalmente en fruta, en el costo muy bajo para la mayor parte de el país.
Plásmido
Los plásmidos, vectores o también llamados plasmidios, son moléculas de ADN extracromosómico circular o lineal que se replican y transcriben independientes del ADN cromosómico. Están presentes normalmente en bacterias, y en algunas ocasiones en organismos eucariotas como las levaduras. Su tamaño varía desde 1 a 250 kb. El número de plásmidos puede variar, dependiendo de su tipo, desde una sola copia hasta algunos cientos por célula. El término plásmido fue presentado por primera vez por el biólogo molecular norteamericano Joshua Lederberg en 1952.1
Las moléculas de ADN plásmidico, adoptan una conformación tipo doble hélice al igual que el ADN de los cromosomas, aunque, por definición, se encuentran fuera de los mismos. Se han encontrado plásmidos en casi todas las bacterias. A diferencia del ADN cromosomal, los plásmidos no tienen proteínas asociadas.
En la mayoría de los casos se considera genético dispensable. Sin embargo, posee información genética importante para las bacterias. Por ejemplo, los genes que codifican para las proteínas que las hace resistentes a los antibióticos están, frecuentemente, en los plásmidos.
Hay algunos plásmidos integrativos, es decir, que tienen la capacidad de insertarse en el cromosoma bacteriano. Estos rompen momentáneamente el cromosoma y se sitúan en su interior, con lo cual, automáticamente la maquinaria celular también reproduce el plásmido. Cuando ese plásmido se ha insertado se les da el nombre de episoma.
Los plásmidos se utilizan en ingeniería genética por su capacidad de reproducirse de manera independiente del ADN cromosomal como así también por que es relativamente fácil manipularlos e insertar nuevas secuencias genéticas.
Los plásmidos usados en Ingeniería Genética suelen contener uno o dos genes que les confieren resistencia a antibióticos y permiten seleccionar clones recombinantes. Hay otros métodos de selección además de la resistencia a antibióticos, como los basados en fluorescencia o en proteínas que destruyen las células sin uso de antibióticos. Estos nuevos métodos de selección de plásmidos son de uso frecuente en agrobiotecnología, debido a la fuerte crítica de grupos ecologistas contra la posibilidad de presencia de antibióticos en los organismos modificados genéticamente.
viernes, 10 de septiembre de 2010
riesgos y beneficios de la modificacion genetica
Ventajas
Mejoras en el proceso industrial
En cuanto a las aplicaciones en agronomía y mejora vegetal en sentido amplio, poseen tres ventajas esenciales:
• Una gran versatilidad en la ingeniería, puesto que los genes que se incorporan al organismo huésped pueden provenir de cualquier especie, incluyendo bacterias.7
• Se puede introducir un solo gen en el organismo sin que esto interfiera con el resto de los genes; de este modo, es ideal para mejorar los caracteres monogénicos, es decir, codificados por un sólo gen, como algunos tipos de resistencias a herbicidas.8
• El proceso de modificación genética demora mucho menos que las técnicas tradicionales de mejoramiento por cruzamiento; la diferencia es de años, en frutales, a meses.
Ventajas para los consumidores
Que fundamentalmente afectan a la calidad del producto final; es decir, a la modificación de sus características.
• Producción de nuevos alimentos
• Posibilidad de incorporar características nutricionales distintas en los alimentos
• Vacunas indiscriminadas comestibles, por ejemplo: tomates con la vacuna de la hepatitis B.9
Ventajas para los agricultores
Mejoras agronómicas relativas a la metodología de producción y su rendimiento.
• Aumento de la productividad y la calidad aparente de los cultivos
• Resistencia a plagas y enfermedades conocidas; por ejemplo, por inclusión de toxinas bacterianas, como las de Bacillus thuringiensis específicas contra determinadas familias de insectos.10
• Tolerancia a herbicidas (como el glifosato o el glufosinato), salinidad, fitoextracción en suelos metalíferos contaminados con metales pesados,11 sequías y temperaturas extremas.[cita requerida]
• Rapidez. El proceso de modificación genética demora mucho menos que las técnicas tradicionales de mejora por cruzamiento, que requiere varias generaciones para eliminar otros genes que se introdujeron en el mismo cruzamiento.[cita requerida]
Ventajas para el ambiente
• Algunas variedades transgénicas han permitido una simplificación en el uso de productos químicos, como en el caso del maíz Bt, donde el combate de plagas ya no requiere el uso de insecticidas químicos de mayor espectro y menor biodegradabilidad.12
Nuevos materiales
Además de la innovación en materia alimentaria, la ingeniería genética permite obtener cualidades novedosas fuera de este ámbito; por ejemplo, por producción de plásticos biodegradables y biocombustibles.13
Inconvenientes
Resistencia a los antibióticos
Para localizar las células en que se ha incorporado y activado el gen introducido, un método común es la introducción de genes que determinan cierta resistencia a unos antibióticos, de modo que al añadir el antibiótico sobreviven solo las células resistentes, con el gen de resistencia incorporado y activo, y probablemente también con el gen que se desea introducir. Dicho método se utiliza con el fin de verificar que el gen de interés haya sido efectivamente incorporado en el genoma del organismo huésped. Estos genes acompañantes son denominados marcadores, y no son necesarios para el resultado final, solo simplifican el proceso para lograrlo. Existen otros marcadores que no tienen relación con la resistencia a quimioterápicos, como los de auxotrofía. Se teme que la inclusión de estos elementos en los alimentos transgénicos podría hacer que la resistencia a los antibioticos se transmitiera a las bacterias de la flora intestinal,14 y de esta a organismos patógenos. No obstante, por orden de la FAO los alimentos transgénicos comercializados deberían carecer de los mencionados genes de resistencia.15
Mayor nivel de residuos tóxicos en los alimentos
• Los cultivos de OMG conllevan un mayor uso de pesticidas. Un estudio basado en los datos del Departamento de Agricultura de los EUA ha demostrado que, en 2008, los cultivos transgénicos han necesitado un 26% más de pesticidas por hectárea que las variedades convencionales.16
• La posibilidad de usar intensivamente insecticidas a los que son resistentes los transgénicos hace que se vean afectadas y dañadas las especies colindantes (no resistentes). No obstante, existen evidencias científicas de que los cultivos de transgénicos resistentes a insecticidas permiten un menor uso de éstos en los campos, lo que redunda en un menor impacto en el ecosistema que alberga al cultivo.17
Posibilidad de generación de nuevas alergias
• Un estudio científico de 1999 mostró la posibilidad de que los alimentos transgénicos produjeran algún tipo de daño. En él se indicaba que el intestino de ratas alimentadas con patatas genéticamente modificadas (expresando una aglutinina de Galanthus nivalis, que es una lectina) resultaba dañado severamente.18 No obstante, este estudio fue criticado debido a la existencia de errores en el diseño experimental y en el manejo de los datos. Por ejemplo, se incluyeron pocos animales en cada grupo experimental (lo que da lugar a una gran incertidumbre estadística), ni se analizó la composición química con precisión de las distintas variedades de patata empleadas, ni se incluyeron controles en los experimentos y finalmente, el análisis estadístico de los resultados era incorrecto.19
Dependencia de la técnica empleada
• La precisión en la obtención de recombinantes, por ejemplo en su localización genómica, es muy dependiente de la técnica empleada: vectores, biobalística, etc.
Contaminación de variedades tradicionales
• El polen de las especies transgéncias puede fecundar a cultivos convencionales, obteniéndose híbridos y transformando a estos cultivos en transgénicos. Este fenomeno ya ocurre con las variedades no transgénicas hoy en día. Esto se conoce como Contaminación genética.2
• La transferencia horizontal a bacterias de la rizosfera, aunque posible, se considera un riesgo remoto.20
Muerte de otros insectos o polinizadores
• Aunque el empleo de recombinantes para toxinas de Bacillus thuringiensis es, por definición, un método específico, a diferencia de los plaguicidas convencionales, existe una demanda comercial que provoca el desarrollo de cepas que actúan conjuntamente contra lepidópteros, coleópteros y dípteros. Este hecho podría afectar a la fauna accesoria del cultivo. [cita requerida]
Impacto ecológico de los cultivos
Tal y como hemos mencionado, algunos autores[cita requerida] suponen que en las especies resistentes a herbicidas los agricultores los emplean en cantidades mayores, con lo cual causan un mayor impacto ambiental. Este posible riesgo ha sido desmentido para algunos OMG, como el maíz resistente a glifosato.21 Sin embargo, un estudio reciente,22 ha mostrado que las formulaciones y productos metabólicos de Roundup causarían la muerte de embriones, placentas, y células umbilicales humanos in vitro aún en bajas concentraciones.
Obligatoriedad del consumo
• La decisión de introducir alimentos transgénicos en la industria alimentaria ha sido totalmente contraria a todo proceso democrático, ocultando incluso la composición de los alimentos. La industria de los OMG sigue estando consciente de que no cuenta con el apoyo de la población de ningún país del mundo, y ello se demuestra con el hecho de que no se revela la información en el envasado de alimentos transgénicos.
Monopolización del mercado, control del agricultor
• Debido a que la misma empresa de OMG provee al agricultor de la planta y de insecticidas o herbicidas, las plantas están adaptadas a dichos productos químicos y viceversa, por lo que el agricultor pasa a depender en exclusiva de una sola empresa proveedora. El monopolio en el suministro conlleva la imposición de precios y condiciones de explotación.
• Como cada OMG está patentado por la multinacional a la que pertenece, el agricultor no puede guardar semillas de su plantación para la siguiente siembra, con lo cual las multinacionales de la biotecnología controlan el mercado de las semillas. Cada año, el agricultor debe hacer una fuerte inversión para obtenerlas.
Mejoras en el proceso industrial
En cuanto a las aplicaciones en agronomía y mejora vegetal en sentido amplio, poseen tres ventajas esenciales:
• Una gran versatilidad en la ingeniería, puesto que los genes que se incorporan al organismo huésped pueden provenir de cualquier especie, incluyendo bacterias.7
• Se puede introducir un solo gen en el organismo sin que esto interfiera con el resto de los genes; de este modo, es ideal para mejorar los caracteres monogénicos, es decir, codificados por un sólo gen, como algunos tipos de resistencias a herbicidas.8
• El proceso de modificación genética demora mucho menos que las técnicas tradicionales de mejoramiento por cruzamiento; la diferencia es de años, en frutales, a meses.
Ventajas para los consumidores
Que fundamentalmente afectan a la calidad del producto final; es decir, a la modificación de sus características.
• Producción de nuevos alimentos
• Posibilidad de incorporar características nutricionales distintas en los alimentos
• Vacunas indiscriminadas comestibles, por ejemplo: tomates con la vacuna de la hepatitis B.9
Ventajas para los agricultores
Mejoras agronómicas relativas a la metodología de producción y su rendimiento.
• Aumento de la productividad y la calidad aparente de los cultivos
• Resistencia a plagas y enfermedades conocidas; por ejemplo, por inclusión de toxinas bacterianas, como las de Bacillus thuringiensis específicas contra determinadas familias de insectos.10
• Tolerancia a herbicidas (como el glifosato o el glufosinato), salinidad, fitoextracción en suelos metalíferos contaminados con metales pesados,11 sequías y temperaturas extremas.[cita requerida]
• Rapidez. El proceso de modificación genética demora mucho menos que las técnicas tradicionales de mejora por cruzamiento, que requiere varias generaciones para eliminar otros genes que se introdujeron en el mismo cruzamiento.[cita requerida]
Ventajas para el ambiente
• Algunas variedades transgénicas han permitido una simplificación en el uso de productos químicos, como en el caso del maíz Bt, donde el combate de plagas ya no requiere el uso de insecticidas químicos de mayor espectro y menor biodegradabilidad.12
Nuevos materiales
Además de la innovación en materia alimentaria, la ingeniería genética permite obtener cualidades novedosas fuera de este ámbito; por ejemplo, por producción de plásticos biodegradables y biocombustibles.13
Inconvenientes
Resistencia a los antibióticos
Para localizar las células en que se ha incorporado y activado el gen introducido, un método común es la introducción de genes que determinan cierta resistencia a unos antibióticos, de modo que al añadir el antibiótico sobreviven solo las células resistentes, con el gen de resistencia incorporado y activo, y probablemente también con el gen que se desea introducir. Dicho método se utiliza con el fin de verificar que el gen de interés haya sido efectivamente incorporado en el genoma del organismo huésped. Estos genes acompañantes son denominados marcadores, y no son necesarios para el resultado final, solo simplifican el proceso para lograrlo. Existen otros marcadores que no tienen relación con la resistencia a quimioterápicos, como los de auxotrofía. Se teme que la inclusión de estos elementos en los alimentos transgénicos podría hacer que la resistencia a los antibioticos se transmitiera a las bacterias de la flora intestinal,14 y de esta a organismos patógenos. No obstante, por orden de la FAO los alimentos transgénicos comercializados deberían carecer de los mencionados genes de resistencia.15
Mayor nivel de residuos tóxicos en los alimentos
• Los cultivos de OMG conllevan un mayor uso de pesticidas. Un estudio basado en los datos del Departamento de Agricultura de los EUA ha demostrado que, en 2008, los cultivos transgénicos han necesitado un 26% más de pesticidas por hectárea que las variedades convencionales.16
• La posibilidad de usar intensivamente insecticidas a los que son resistentes los transgénicos hace que se vean afectadas y dañadas las especies colindantes (no resistentes). No obstante, existen evidencias científicas de que los cultivos de transgénicos resistentes a insecticidas permiten un menor uso de éstos en los campos, lo que redunda en un menor impacto en el ecosistema que alberga al cultivo.17
Posibilidad de generación de nuevas alergias
• Un estudio científico de 1999 mostró la posibilidad de que los alimentos transgénicos produjeran algún tipo de daño. En él se indicaba que el intestino de ratas alimentadas con patatas genéticamente modificadas (expresando una aglutinina de Galanthus nivalis, que es una lectina) resultaba dañado severamente.18 No obstante, este estudio fue criticado debido a la existencia de errores en el diseño experimental y en el manejo de los datos. Por ejemplo, se incluyeron pocos animales en cada grupo experimental (lo que da lugar a una gran incertidumbre estadística), ni se analizó la composición química con precisión de las distintas variedades de patata empleadas, ni se incluyeron controles en los experimentos y finalmente, el análisis estadístico de los resultados era incorrecto.19
Dependencia de la técnica empleada
• La precisión en la obtención de recombinantes, por ejemplo en su localización genómica, es muy dependiente de la técnica empleada: vectores, biobalística, etc.
Contaminación de variedades tradicionales
• El polen de las especies transgéncias puede fecundar a cultivos convencionales, obteniéndose híbridos y transformando a estos cultivos en transgénicos. Este fenomeno ya ocurre con las variedades no transgénicas hoy en día. Esto se conoce como Contaminación genética.2
• La transferencia horizontal a bacterias de la rizosfera, aunque posible, se considera un riesgo remoto.20
Muerte de otros insectos o polinizadores
• Aunque el empleo de recombinantes para toxinas de Bacillus thuringiensis es, por definición, un método específico, a diferencia de los plaguicidas convencionales, existe una demanda comercial que provoca el desarrollo de cepas que actúan conjuntamente contra lepidópteros, coleópteros y dípteros. Este hecho podría afectar a la fauna accesoria del cultivo. [cita requerida]
Impacto ecológico de los cultivos
Tal y como hemos mencionado, algunos autores[cita requerida] suponen que en las especies resistentes a herbicidas los agricultores los emplean en cantidades mayores, con lo cual causan un mayor impacto ambiental. Este posible riesgo ha sido desmentido para algunos OMG, como el maíz resistente a glifosato.21 Sin embargo, un estudio reciente,22 ha mostrado que las formulaciones y productos metabólicos de Roundup causarían la muerte de embriones, placentas, y células umbilicales humanos in vitro aún en bajas concentraciones.
Obligatoriedad del consumo
• La decisión de introducir alimentos transgénicos en la industria alimentaria ha sido totalmente contraria a todo proceso democrático, ocultando incluso la composición de los alimentos. La industria de los OMG sigue estando consciente de que no cuenta con el apoyo de la población de ningún país del mundo, y ello se demuestra con el hecho de que no se revela la información en el envasado de alimentos transgénicos.
Monopolización del mercado, control del agricultor
• Debido a que la misma empresa de OMG provee al agricultor de la planta y de insecticidas o herbicidas, las plantas están adaptadas a dichos productos químicos y viceversa, por lo que el agricultor pasa a depender en exclusiva de una sola empresa proveedora. El monopolio en el suministro conlleva la imposición de precios y condiciones de explotación.
• Como cada OMG está patentado por la multinacional a la que pertenece, el agricultor no puede guardar semillas de su plantación para la siguiente siembra, con lo cual las multinacionales de la biotecnología controlan el mercado de las semillas. Cada año, el agricultor debe hacer una fuerte inversión para obtenerlas.
introduccion
en este blog veremos los temas de genetica en la actualidad, se empezara con lo pricipal que seria la estructura y composicion del dna,cromosomas,genes,y cariotipos.y en los cariotipos se vra el analisis de estos mismos.
despues veremos para que sirve el dna como lo son las tecnicas de dna que sirven para medicina,pruebas de paternidad,forencia,etc.despues ya en otro tema es la modficacion genetica que se vera en tres etapas: riesgos y beneficios, sus usos y por ultimoi clonacion en animales y plantas.
despues veremos para que sirve el dna como lo son las tecnicas de dna que sirven para medicina,pruebas de paternidad,forencia,etc.despues ya en otro tema es la modficacion genetica que se vera en tres etapas: riesgos y beneficios, sus usos y por ultimoi clonacion en animales y plantas.
domingo, 22 de agosto de 2010
tecnicas de analisis de dna
ADN PROFILING
El análisis de ADN (también llamada prueba de ADN, escribiendo ADN o huellas genéticas) es una técnica empleada por los científicos forenses para ayudar en la identificación de los individuos sobre la base de sus respectivos ADN perfiles. perfiles de ADN se cifran conjuntos de números que reflejan la persona del ADN de una maquillaje, que también puede ser utilizado como identificador de la persona. el análisis de ADN no debe confundirse con la secuenciación del genoma completo . Se utiliza, por ejemplo, pruebas de los padres y la violación de investigación .
Aunque el 99,9% de las secuencias de ADN humano son los mismos en cada persona, lo suficiente del ADN es diferente para distinguir un individuo de otro. utiliza el análisis de ADN repetitivo ("repetir") secuencias que son muy variables, llamada variable número de repeticiones en tándem (VNTR). VNTR loci son muy similares entre los humanos relacionados de cerca, pero tan variables que los individuos no relacionados son extremadamente poco probable que tenga la misma VNTR.
Los perfiles de ADN técnica fue reportada por primera vez en 1984 por Sir Alec Jeffreys en la Universidad de Leicester en Inglaterra, y ahora es la base de varias bases de datos nacional de ADN . la caracterización genética Dr. Jeffreys fue comercializada en 1987, cuando una empresa química ICI, inició un centro de sangre-prueba en Inglaterra.
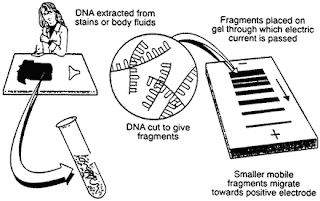
análisis de RFLP
Los primeros métodos para averiguar la genética utilizada para perfiles de ADN implicadas enzimas de restricción digestión, seguida por Southern blot análisis. A pesar de polimorfismos pueden existir en la división sitios enzima de restricción, más comúnmente las enzimas y las sondas de ADN se utiliza para analizar loci VNTR. Sin embargo, la técnica de Southern blot es laborioso, y requiere grandes cantidades de ADN de muestras no degradadas. Además, la técnica original de Brown Karl miró muchas minisatélite loci, al mismo tiempo, el aumento de la variabilidad observada, pero lo que hace difícil discernir alelos individuales (y por tanto se opone a las pruebas los padres ). Estas técnicas principios han sido suplantadas por las pruebas de PCR-based.
análisis de PCR
Con la invención de la reacción en cadena de la polimerasa (PCR), el análisis de ADN dieron pasos de gigante, tanto en poder de discriminación y la capacidad de recuperar información desde muy pequeño (o degradado) muestras de partida. PCR amplifica considerablemente los importes de una región específica del ADN, utilizando oligonucleótidos cebadores y una ADN polimerasa termoestable . Los primeros ensayos, como el HLA - DQ alfa inversa dot blot tiras llegó a ser muy popular debido a su facilidad de uso y la rapidez con que podría ser un resultado obtenido. Sin embargo no eran tan exigentes como RFLP. También era difícil determinar un perfil de ADN de las muestras mixtas, como una esponja vaginal de una víctima de asalto sexual.
Afortunadamente, el método PCR es fácilmente adaptable para el análisis de los loci VNTR. En los Estados Unidos el FBI ha estandarizado un conjunto de 13 ensayos VNTR para la tipificación del ADN, y ha organizado el CODIS base de datos para la identificación forense en casos penales. ensayos similares, así como bases de datos se han creado en otros países. Además, los kits comerciales disponibles que analizan polimorfismos de un solo nucleótido (SNPs). Estos kits utilizan la PCR para amplificar regiones específicas con variaciones conocidas y hibridan a sondas ancladas en las tarjetas, que se traduce en una mancha de color correspondiente a la variación de la secuencia en particular.
El análisis de ADN (también llamada prueba de ADN, escribiendo ADN o huellas genéticas) es una técnica empleada por los científicos forenses para ayudar en la identificación de los individuos sobre la base de sus respectivos ADN perfiles. perfiles de ADN se cifran conjuntos de números que reflejan la persona del ADN de una maquillaje, que también puede ser utilizado como identificador de la persona. el análisis de ADN no debe confundirse con la secuenciación del genoma completo . Se utiliza, por ejemplo, pruebas de los padres y la violación de investigación .
Aunque el 99,9% de las secuencias de ADN humano son los mismos en cada persona, lo suficiente del ADN es diferente para distinguir un individuo de otro. utiliza el análisis de ADN repetitivo ("repetir") secuencias que son muy variables, llamada variable número de repeticiones en tándem (VNTR). VNTR loci son muy similares entre los humanos relacionados de cerca, pero tan variables que los individuos no relacionados son extremadamente poco probable que tenga la misma VNTR.
Los perfiles de ADN técnica fue reportada por primera vez en 1984 por Sir Alec Jeffreys en la Universidad de Leicester en Inglaterra, y ahora es la base de varias bases de datos nacional de ADN . la caracterización genética Dr. Jeffreys fue comercializada en 1987, cuando una empresa química ICI, inició un centro de sangre-prueba en Inglaterra.
análisis de RFLP
Los primeros métodos para averiguar la genética utilizada para perfiles de ADN implicadas enzimas de restricción digestión, seguida por Southern blot análisis. A pesar de polimorfismos pueden existir en la división sitios enzima de restricción, más comúnmente las enzimas y las sondas de ADN se utiliza para analizar loci VNTR. Sin embargo, la técnica de Southern blot es laborioso, y requiere grandes cantidades de ADN de muestras no degradadas. Además, la técnica original de Brown Karl miró muchas minisatélite loci, al mismo tiempo, el aumento de la variabilidad observada, pero lo que hace difícil discernir alelos individuales (y por tanto se opone a las pruebas los padres ). Estas técnicas principios han sido suplantadas por las pruebas de PCR-based.
análisis de PCR
Con la invención de la reacción en cadena de la polimerasa (PCR), el análisis de ADN dieron pasos de gigante, tanto en poder de discriminación y la capacidad de recuperar información desde muy pequeño (o degradado) muestras de partida. PCR amplifica considerablemente los importes de una región específica del ADN, utilizando oligonucleótidos cebadores y una ADN polimerasa termoestable . Los primeros ensayos, como el HLA - DQ alfa inversa dot blot tiras llegó a ser muy popular debido a su facilidad de uso y la rapidez con que podría ser un resultado obtenido. Sin embargo no eran tan exigentes como RFLP. También era difícil determinar un perfil de ADN de las muestras mixtas, como una esponja vaginal de una víctima de asalto sexual.
Afortunadamente, el método PCR es fácilmente adaptable para el análisis de los loci VNTR. En los Estados Unidos el FBI ha estandarizado un conjunto de 13 ensayos VNTR para la tipificación del ADN, y ha organizado el CODIS base de datos para la identificación forense en casos penales. ensayos similares, así como bases de datos se han creado en otros países. Además, los kits comerciales disponibles que analizan polimorfismos de un solo nucleótido (SNPs). Estos kits utilizan la PCR para amplificar regiones específicas con variaciones conocidas y hibridan a sondas ancladas en las tarjetas, que se traduce en una mancha de color correspondiente a la variación de la secuencia en particular.
miércoles, 18 de agosto de 2010
Inversión de Cromosomas
Una inversión consiste en dos roturas en un cromosoma. El área entre las roturas se invierte gira, y entonces se reinserta y las roturas entonces quedan unidas al resto del cromosoma. Si el área invertida incluye el centrómero se llama inversión pericéntrica,. Si no, se llama inversión paracéntrica.
Dense cuenta que en una inversión pericéntrica una rotura está en el brazo corto y una en el brazo largo. Por lo tanto un ejemplo de una nomenclatura citogenétoca puede leerse 24, XY,inv(3)(p23q27). Una inversión paracéntrica no incluye el centrómero y un ejemplo podría ser 46,XY,inv(1)(p12p31).
Cuando un padre tiene una inversión hay un incremento del riesgo para la descendencia con una incorrecta cantidad de material genético. Esto puede conducir a tener niños con defectos de nacimiento y/o anormal desarrollo o un incremento del riesgo de aborto. El posible resultado de un embarazo para un individuo con una inversión es bastante complicado y depende de lo grande que sea la inversión, dónde esté, y qué tipo de inversión está presente, parecéntrica o pericentrica. Hay muchas inversiones que ocurren en la población general que son llamadas variantes normales. Incluida inv(9) y inv(2). Estas inversiones no son relacionadas en un incremento de riesgo de defectos en el nacimiento y/o dificultades en el desarrollo.
Cariotipo espectral
El análisis espectral de los cariotipos (o SKY) se trata de una tecnología de citogenética molecular que permite el estudio y visualización de los 23 pares de cromosomas en forma simultánea. Sondas marcadas fluorescentemente son hechas para cada cromosoma al marcar DNA especifico de cada cromosoma con diferentes fluoroforos. Debido a que hay un limitado número de fluoroforos espectralmente distintos , un método de etiquetado combinatorio es usado para generar muchos colores diferentes. La diferencias espectrales generadas por el etiquetado combinatorio son capturadas y analizadas usando un interferómetro agregado a un microscopio de fluorescencia. El programa de procesamiento de imágenes entonces asigna un pseudocolor a cada combinación espectralmente diferente, permitiendo la visualización de cromosomas coloreados.4
Esta técnica es usada para identificar aberraciones estructurales cromosomicas en células cancerigenas y otras patologías cuando el bandeo con Giemsa u otras técnicas no son lo suficientemente precisas. no son suficientemente seguras
Este tipo de técnicas mejorará la identificación y diagnóstico de las aberraciones cromosómicas en citogenética prenatal así como en células cancerosas.
Síndrome de Turner
El síndrome Turner, síndrome Ullrich-Turner o monosomía X es una enfermedad genética caracterizada por la presencia de un solo cromosoma X. Genotípicamente son mujeres (por ausencia de cromosoma Y). A las mujeres con síndrome de Turner les falta parte o todo un cromosoma X. En algunos casos se produce mosaicismo, es decir que la falta de cromosoma X no afecta a todas las células del cuerpo.1
La ausencia de cromosoma Y determina el sexo femenino de todos los individuos afectados, y la ausencia del segundo cromosoma X determina la falta de desarrollo de los caracteres sexuales primarios y secundarios. Esto confiere a las mujeres que padecen el síndrome de Turner un aspecto infantil e infertilidad de por vida. Incide, aproximadamente, en 1 de cada 2.500 niñas.
El nombre "síndrome Turner" proviene del médico Dr. Henry Turner, quien fue el primero en describir el conjunto de descubrimientos en 1938. No fue sino hasta 1959 que se identificó la causa del síndrome Turner (la presencia de un sólo cromosoma X). Otros nombres alternativos son síndrome Bonnevie-Ullrich
Síndrome de Klinefelter
El síndrome de Klinefelter es una anomalía cromosómica que afecta solamente a los hombres y ocasiona hipogonadismo.
El sexo de las personas está determinado por los cromosomas X e Y. Los hombres tienen los cromosomas 44XY (46) y las mujeres tienen los cromosomas 44XX (46). En el síndrome de Klinefelter se pueden presentar los cromosomas 44XXY (47), 44XXXY (48), 44XXYY(48), 44XXXXY (49), etc y los llamados "mosaicos" o "mosaicismos" 46XY / 47XXY.
Es una alteración genética que se desarrolla por la separación incorrecta de los cromosomas homólogos durante las meiosis que dan lugar a los gametos de uno de los progenitores, aunque también puede darse en las primeras divisiones del cigoto.
Se cree que Carlos II de España sufrió este síndrome, debido fundamentalmente a los sucesivos matrimonios endogámicos de sus antepasados y falta de sangre nueva.
Una inversión consiste en dos roturas en un cromosoma. El área entre las roturas se invierte gira, y entonces se reinserta y las roturas entonces quedan unidas al resto del cromosoma. Si el área invertida incluye el centrómero se llama inversión pericéntrica,. Si no, se llama inversión paracéntrica.
Dense cuenta que en una inversión pericéntrica una rotura está en el brazo corto y una en el brazo largo. Por lo tanto un ejemplo de una nomenclatura citogenétoca puede leerse 24, XY,inv(3)(p23q27). Una inversión paracéntrica no incluye el centrómero y un ejemplo podría ser 46,XY,inv(1)(p12p31).
Cuando un padre tiene una inversión hay un incremento del riesgo para la descendencia con una incorrecta cantidad de material genético. Esto puede conducir a tener niños con defectos de nacimiento y/o anormal desarrollo o un incremento del riesgo de aborto. El posible resultado de un embarazo para un individuo con una inversión es bastante complicado y depende de lo grande que sea la inversión, dónde esté, y qué tipo de inversión está presente, parecéntrica o pericentrica. Hay muchas inversiones que ocurren en la población general que son llamadas variantes normales. Incluida inv(9) y inv(2). Estas inversiones no son relacionadas en un incremento de riesgo de defectos en el nacimiento y/o dificultades en el desarrollo.
Cariotipo espectral
El análisis espectral de los cariotipos (o SKY) se trata de una tecnología de citogenética molecular que permite el estudio y visualización de los 23 pares de cromosomas en forma simultánea. Sondas marcadas fluorescentemente son hechas para cada cromosoma al marcar DNA especifico de cada cromosoma con diferentes fluoroforos. Debido a que hay un limitado número de fluoroforos espectralmente distintos , un método de etiquetado combinatorio es usado para generar muchos colores diferentes. La diferencias espectrales generadas por el etiquetado combinatorio son capturadas y analizadas usando un interferómetro agregado a un microscopio de fluorescencia. El programa de procesamiento de imágenes entonces asigna un pseudocolor a cada combinación espectralmente diferente, permitiendo la visualización de cromosomas coloreados.4
Esta técnica es usada para identificar aberraciones estructurales cromosomicas en células cancerigenas y otras patologías cuando el bandeo con Giemsa u otras técnicas no son lo suficientemente precisas. no son suficientemente seguras
Este tipo de técnicas mejorará la identificación y diagnóstico de las aberraciones cromosómicas en citogenética prenatal así como en células cancerosas.
Síndrome de Turner
El síndrome Turner, síndrome Ullrich-Turner o monosomía X es una enfermedad genética caracterizada por la presencia de un solo cromosoma X. Genotípicamente son mujeres (por ausencia de cromosoma Y). A las mujeres con síndrome de Turner les falta parte o todo un cromosoma X. En algunos casos se produce mosaicismo, es decir que la falta de cromosoma X no afecta a todas las células del cuerpo.1
La ausencia de cromosoma Y determina el sexo femenino de todos los individuos afectados, y la ausencia del segundo cromosoma X determina la falta de desarrollo de los caracteres sexuales primarios y secundarios. Esto confiere a las mujeres que padecen el síndrome de Turner un aspecto infantil e infertilidad de por vida. Incide, aproximadamente, en 1 de cada 2.500 niñas.
El nombre "síndrome Turner" proviene del médico Dr. Henry Turner, quien fue el primero en describir el conjunto de descubrimientos en 1938. No fue sino hasta 1959 que se identificó la causa del síndrome Turner (la presencia de un sólo cromosoma X). Otros nombres alternativos son síndrome Bonnevie-Ullrich
Síndrome de Klinefelter
El síndrome de Klinefelter es una anomalía cromosómica que afecta solamente a los hombres y ocasiona hipogonadismo.
El sexo de las personas está determinado por los cromosomas X e Y. Los hombres tienen los cromosomas 44XY (46) y las mujeres tienen los cromosomas 44XX (46). En el síndrome de Klinefelter se pueden presentar los cromosomas 44XXY (47), 44XXXY (48), 44XXYY(48), 44XXXXY (49), etc y los llamados "mosaicos" o "mosaicismos" 46XY / 47XXY.
Es una alteración genética que se desarrolla por la separación incorrecta de los cromosomas homólogos durante las meiosis que dan lugar a los gametos de uno de los progenitores, aunque también puede darse en las primeras divisiones del cigoto.
Se cree que Carlos II de España sufrió este síndrome, debido fundamentalmente a los sucesivos matrimonios endogámicos de sus antepasados y falta de sangre nueva.
cariotipos
El cariotipo es un esquema, foto o dibujo de los cromosomas de una célula metafásica ordenados de acuerdo a su morfología (metacéntricos, submetacéntricos, telocéntricos, subtelocéntricos y acrocéntricos) y tamaño, que están caracterizados y representan a todos los individuos de una especie. El cariotipo es característico de cada especie, al igual que el número de cromosomas; el ser humano tiene 46 cromosomas (23 pares porque somos diploides o 2n) en el núcleo de cada célula,1 organizados en 22 pares autosómicos y 1 par sexual (hombre XY y mujer XX).Cada brazo ha sido dividido en zonas y cada zona, a su vez, en bandas e incluso las bandas en subbandas, gracias a las técnicas de marcado. No obstante puede darse el caso, en humanos, de que existan otros patrones en los cariotipos, a lo cual se le conoce como aberración cromosómica.
Mediante el cariotipado se pueden analizar anomalías numéricas y estructurales, cosa que sería muy difícil de observar mediante genética mendeliana.
Número de cromosomas en cada serie
Un ejemplo de la variabilidad entre especies estrechamente relacionadas es el de muntjac, que fue investigado por Kurt Benirschke y su compañero Doris Wurster donde demostraron que el número diploide del muntjac Chino (Muntiacus reevesi) resultó ser de 46 y todos telocéntricos. Cuando se estudió el cariotipo del muntjac Indio (Muntiacus muntjak) vieron que la hembra tenía 6 y el macho 7 cromosomas.14 "Ellos simplemente no podían creer lo que habían visto... Ellos se mantuvieron en silencio por dos o tres años porque ellos pensaban que algo había andado mal con su cultivo de tejidos... Pero cuando ellos obtuvieron un par más de especimenes, ellos confirmaron sus hallazgos".15
El número de cromosomas en el cariotipo entre especies no relacionadas es enormemente variable.
El record más bajo le pertenece al nematodo Parascaris univalens, donde el número haploide es n = 1; el record más alto podría estar en algún lugar entre los helechos, con el helecho Lengua de Adder Ophioglossum adelante con un promedio de 1262 cromosomas.16
El más alto score para animales podría estar entre el esturión de nariz corta Acipenser brevirostrum con solamente 372 cromosomas.17
La existencia de cromosomas supernumerarios o B significa que el número de cromosomas puede variar incluso dentro de una misma población. (El cromosoma supernumerario se sitúa en el lugar del cromosoma normal 21. La fórmula de este triple cromosoma puede ser XXY o XYY).
Todos los seres humanos tienen 22 pares de cromosomas iguales, denominados autosomas, y un par de cromosomas diferentes según el sexo del individuo, los cromosomas sexuales o heterocromosomas.
Los cromosomas de cada especie poseen una serie de características, como la forma, el tamaño, la posición del centrómero y las bandas que presentan al teñirse. Este conjunto de particularidades, que permite identificar los cromosomas de las distintas especies, recibe el nombre de cariotipo, y su representación gráfica, ordenada por parejas de cromosomas homólogos, se denomina cariograma.
Es recomendable realizar un cariotipo de un individuo en los casos que a continuación se exponen:Para confirmar síndromes congénitos.
• Cuando se observan algunas anomalías específicas o que pueden estar relacionadas con los heterocromosomas.
• En situaciones de abortos repetidos, problemas de esterilidad...
Mediante el estudio del cariotipo es posible detectar anomalías en el número o en la forma de los cromosomas. La mayoría de estas anomalías provocan deficiencias, y muchos individuos no llegan a nacer o mueren en los primeros meses de vida. La determinación del cariotipo del feto permite detectar, antes del nacimiento, algunas de estas deficiencias.
Para determinar el cariotipo de un individuo, es necesario llevar a cabo un cultivo de células y, cuando estas comienzan a dividirse, teñirlas y hacer una preparación microscópica para fotografiar los cromosomas.
En un feto, las células se pueden obtener por amniocentesis, es decir, efectuando una punción en el vientre de la madre para obtener líquido amniótico o bien por punción directa del cordón umbilical para extraer sangre del feto. En un individuo adulto se utilizan los glóbulos blancos de la sangre.
El último paso para determinar el cariotipo es ordenar y emparejar los cromosomas, y verificar si es correcto.
Mediante el cariotipado se pueden analizar anomalías numéricas y estructurales, cosa que sería muy difícil de observar mediante genética mendeliana.
Número de cromosomas en cada serie
Un ejemplo de la variabilidad entre especies estrechamente relacionadas es el de muntjac, que fue investigado por Kurt Benirschke y su compañero Doris Wurster donde demostraron que el número diploide del muntjac Chino (Muntiacus reevesi) resultó ser de 46 y todos telocéntricos. Cuando se estudió el cariotipo del muntjac Indio (Muntiacus muntjak) vieron que la hembra tenía 6 y el macho 7 cromosomas.14 "Ellos simplemente no podían creer lo que habían visto... Ellos se mantuvieron en silencio por dos o tres años porque ellos pensaban que algo había andado mal con su cultivo de tejidos... Pero cuando ellos obtuvieron un par más de especimenes, ellos confirmaron sus hallazgos".15
El número de cromosomas en el cariotipo entre especies no relacionadas es enormemente variable.
El record más bajo le pertenece al nematodo Parascaris univalens, donde el número haploide es n = 1; el record más alto podría estar en algún lugar entre los helechos, con el helecho Lengua de Adder Ophioglossum adelante con un promedio de 1262 cromosomas.16
El más alto score para animales podría estar entre el esturión de nariz corta Acipenser brevirostrum con solamente 372 cromosomas.17
La existencia de cromosomas supernumerarios o B significa que el número de cromosomas puede variar incluso dentro de una misma población. (El cromosoma supernumerario se sitúa en el lugar del cromosoma normal 21. La fórmula de este triple cromosoma puede ser XXY o XYY).
Todos los seres humanos tienen 22 pares de cromosomas iguales, denominados autosomas, y un par de cromosomas diferentes según el sexo del individuo, los cromosomas sexuales o heterocromosomas.
Los cromosomas de cada especie poseen una serie de características, como la forma, el tamaño, la posición del centrómero y las bandas que presentan al teñirse. Este conjunto de particularidades, que permite identificar los cromosomas de las distintas especies, recibe el nombre de cariotipo, y su representación gráfica, ordenada por parejas de cromosomas homólogos, se denomina cariograma.
Es recomendable realizar un cariotipo de un individuo en los casos que a continuación se exponen:Para confirmar síndromes congénitos.
• Cuando se observan algunas anomalías específicas o que pueden estar relacionadas con los heterocromosomas.
• En situaciones de abortos repetidos, problemas de esterilidad...
Mediante el estudio del cariotipo es posible detectar anomalías en el número o en la forma de los cromosomas. La mayoría de estas anomalías provocan deficiencias, y muchos individuos no llegan a nacer o mueren en los primeros meses de vida. La determinación del cariotipo del feto permite detectar, antes del nacimiento, algunas de estas deficiencias.
Para determinar el cariotipo de un individuo, es necesario llevar a cabo un cultivo de células y, cuando estas comienzan a dividirse, teñirlas y hacer una preparación microscópica para fotografiar los cromosomas.
En un feto, las células se pueden obtener por amniocentesis, es decir, efectuando una punción en el vientre de la madre para obtener líquido amniótico o bien por punción directa del cordón umbilical para extraer sangre del feto. En un individuo adulto se utilizan los glóbulos blancos de la sangre.
El último paso para determinar el cariotipo es ordenar y emparejar los cromosomas, y verificar si es correcto.
lunes, 9 de agosto de 2010
Answer the questions:
The table shows the base composition of genetic material from ten sources.
Source of genetic material Base composition (%)
Adenine Guanine Thymine Cytosine Uracil
Cattle thymus gland 28.2 21.5 27.8 22.5 0.0
Cattle spleen 27.9 22.7 27.3 22.1 0.0
Cattle sperm 28.7 22.2 27.2 22.0 0.0
Pig thymus gland 30.0 20.4 28.9 20.7 0.0
Salmon 29.7 20.8 29.1 20.4 0.0
Wheat 27.3 22.7 27.1 22.8 0.0
Yeast 31.3 18.7 32.9 17.1 0.0
E coli (bacteria) 26.0 24.9 23.9 25.2 0.0
Human sperm 31.0 19.1 31.5 18.4 0.0
Influenza virus 23.0 20.0 0.00 24.5 32.5
A) Deducir el tipo de material genético usado por
• Ganado
• E.coli
• Virus de gripe
B) Sugerir una razón de la diferencia entre el Ganado thymus la glándula, el Bazo y la esperma en las medidas de su composición baja.
C) - Explican los motivos para la cantidad total de adenine más guanine que ser cerca del 50 % en el material genético de mucha de la especie en la mesa.
_Identify dos otras tendencias en la composición baja de la especie que tienen el 50 % adenine y guanine.
D) _ Identifican una especie mostrada en la mesa que no sigue las tendencias en la composición baja descrita en C)
_ Explicar los motivos para la composición baja de este siendo diferente de especie.
Desarrollo
A)
GANADO: el ganado tiene como material genético el ADN por que como muestra la tabla vemos que posee timina y que no posee uracilo y como ya lo sabemos el ADN consta de timina.
E.COLI: por las mismas razones del ganado este también utiliza ADN como material genético por q posee timina y no uracilo.
VIRUS DE GRIPE: ya rompiendo los esquemas este usa de material genético el rna por que es al contrario de los dos anteriores, porque en vez de tener timina tiene uracilo y el uracilo solo lo tiene el rna
B)
C)
*) Porque la adenina mas guanina crean las purinas que estas están más presentes en las comidas que diariamente los humanos comen.
*) Cattle thymus gland 28.2 21.5 = 49.7
Influenza virus 23.0 20.0 = 43.0
D)
Como ya sabemos la influenza virus tiene de material genético el RNA y para poder ser RNA tiene que tener más citosina para poder tener bastante timina
The table shows the base composition of genetic material from ten sources.
Source of genetic material Base composition (%)
Adenine Guanine Thymine Cytosine Uracil
Cattle thymus gland 28.2 21.5 27.8 22.5 0.0
Cattle spleen 27.9 22.7 27.3 22.1 0.0
Cattle sperm 28.7 22.2 27.2 22.0 0.0
Pig thymus gland 30.0 20.4 28.9 20.7 0.0
Salmon 29.7 20.8 29.1 20.4 0.0
Wheat 27.3 22.7 27.1 22.8 0.0
Yeast 31.3 18.7 32.9 17.1 0.0
E coli (bacteria) 26.0 24.9 23.9 25.2 0.0
Human sperm 31.0 19.1 31.5 18.4 0.0
Influenza virus 23.0 20.0 0.00 24.5 32.5
A) Deducir el tipo de material genético usado por
• Ganado
• E.coli
• Virus de gripe
B) Sugerir una razón de la diferencia entre el Ganado thymus la glándula, el Bazo y la esperma en las medidas de su composición baja.
C) - Explican los motivos para la cantidad total de adenine más guanine que ser cerca del 50 % en el material genético de mucha de la especie en la mesa.
_Identify dos otras tendencias en la composición baja de la especie que tienen el 50 % adenine y guanine.
D) _ Identifican una especie mostrada en la mesa que no sigue las tendencias en la composición baja descrita en C)
_ Explicar los motivos para la composición baja de este siendo diferente de especie.
Desarrollo
A)
GANADO: el ganado tiene como material genético el ADN por que como muestra la tabla vemos que posee timina y que no posee uracilo y como ya lo sabemos el ADN consta de timina.
E.COLI: por las mismas razones del ganado este también utiliza ADN como material genético por q posee timina y no uracilo.
VIRUS DE GRIPE: ya rompiendo los esquemas este usa de material genético el rna por que es al contrario de los dos anteriores, porque en vez de tener timina tiene uracilo y el uracilo solo lo tiene el rna
B)
C)
*) Porque la adenina mas guanina crean las purinas que estas están más presentes en las comidas que diariamente los humanos comen.
*) Cattle thymus gland 28.2 21.5 = 49.7
Influenza virus 23.0 20.0 = 43.0
D)
Como ya sabemos la influenza virus tiene de material genético el RNA y para poder ser RNA tiene que tener más citosina para poder tener bastante timina
estructura del dna,cromosomas y gen
Un gen es una sección de la cadena de ADN que lleva las instrucciones de una función específica. Por ejemplo, los genes de la 'globina' contienen instrucciones para la construcción de la proteína hemoglobina, que es la que permite a nuestra sangre llevar el oxígeno por todo el cuerpo. Los humanos tienen alrededor de 50.000 genes diferentes, los cuales trabajan juntos de forma compleja para controlar mucho de lo que hace nuestro cuerpo. Aunque todos tengamos los mismos genes, hay diferentes versiones de muchos de ellos, llamados alelos. Por ejemplo, mientras que la mayoría de la gente tiene genes que les dan iris pigmentados (de color), existen múltiples alelos para colores específicos. Cada persona tiene una combinación particular de alelos para el color de ojos, el color del pelo, etc., lo cual los convierte en genéticamente únicos.
Estructura externa de los cromosomas:
El estudio de la estructura externa de los cromosomas de cualquier especie eucariótica consiste en analizar la forma, tamaño y número de los cromosomas que posee. El mejor momento para llevar a cabo dicho estudio suele ser aquel en el que los cromosomas han alcanzado su máximo grado de contracción y tienen sus bordes perfectamente definidos. Dicho momento suele ser la metafase mitótica. El estudio de la estructura externa de los cromosomas culmina con la obtención del cariotipo. Los cromosomas se pueden estudiar en distintos momentos según la especie y dependiendo de los objetivos planteados. Algunas especies tienen cromosomas que se pueden observar con gran detalle en interfase, tal es el caso de Drosophila melanogaster, que posee cromosomas politénicos gigantes que se observan en las glándulas salivales de dicho insecto, y el de Chironomus tentans, otro díptero. El cariotipo se confecciona usualmente después de un apropiado pre-tratamiento y tinción de las células, para hacer más visibles los cromosomas individuales. Al diagrama simplificado de los cromosomas metafásicos del cariotipo se lo denomina idiograma, que se construye con el número genómico. Para realizar el ordenamiento de los cromosomas tanto en cariotipos como idiogramas se debe tener en cuenta el tamaño cromosómico (ubicados de mayor a menor, con el brazo corto “bc” o "p" hacia arriba y el brazo largo “bl” o "q" hacia abajo); posición del centrómero (generalmente alineados) y presencia de constricciones secundarias y satélites.
Estructura del ADN.
Las cuatro bases nitrogenadas del ADN se encuentran distribuidas a lo largo de la "columna vertebral" que conforman los azúcares con el ácido fosfórico en un orden particular. (la secuencia del ADN). La adenina(A) se empareja con la timina (T), mientras que la citosina (C) lo hace con la guanina. Las dos hebras de ADN se matienen juntas por los puentes hidrógenos entre las base.
16:33
Estructura externa de los cromosomas:
El estudio de la estructura externa de los cromosomas de cualquier especie eucariótica consiste en analizar la forma, tamaño y número de los cromosomas que posee. El mejor momento para llevar a cabo dicho estudio suele ser aquel en el que los cromosomas han alcanzado su máximo grado de contracción y tienen sus bordes perfectamente definidos. Dicho momento suele ser la metafase mitótica. El estudio de la estructura externa de los cromosomas culmina con la obtención del cariotipo. Los cromosomas se pueden estudiar en distintos momentos según la especie y dependiendo de los objetivos planteados. Algunas especies tienen cromosomas que se pueden observar con gran detalle en interfase, tal es el caso de Drosophila melanogaster, que posee cromosomas politénicos gigantes que se observan en las glándulas salivales de dicho insecto, y el de Chironomus tentans, otro díptero. El cariotipo se confecciona usualmente después de un apropiado pre-tratamiento y tinción de las células, para hacer más visibles los cromosomas individuales. Al diagrama simplificado de los cromosomas metafásicos del cariotipo se lo denomina idiograma, que se construye con el número genómico. Para realizar el ordenamiento de los cromosomas tanto en cariotipos como idiogramas se debe tener en cuenta el tamaño cromosómico (ubicados de mayor a menor, con el brazo corto “bc” o "p" hacia arriba y el brazo largo “bl” o "q" hacia abajo); posición del centrómero (generalmente alineados) y presencia de constricciones secundarias y satélites.
Estructura del ADN.
Las cuatro bases nitrogenadas del ADN se encuentran distribuidas a lo largo de la "columna vertebral" que conforman los azúcares con el ácido fosfórico en un orden particular. (la secuencia del ADN). La adenina(A) se empareja con la timina (T), mientras que la citosina (C) lo hace con la guanina. Las dos hebras de ADN se matienen juntas por los puentes hidrógenos entre las base.
16:33
lunes, 2 de agosto de 2010
jueves, 29 de julio de 2010
Suscribirse a:
Comentarios (Atom)